GIỚI THIỆU BÀI HỌC
Bài giảng Bài tập Amin - Phần 2 bao gồm các dạng bài tập về công thức cấu tạo, tính chất hóa học và nhận biết Amin. Đến với bài giảng các em sẽ được rèn luyện và nâng cao kỹ năng, phương pháp giải các dạng bài tập.
NỘI DUNG BÀI HỌC
Bài tập 1: Đốt cháy hoàn toàn amin no đơn chức X, thu được 16,8 lít CO2; 2,8 lít N2 (đktc) và 20,25 gam H2O. Công thức phân tử của X là
A. C4H9N. B. C3H7N. C. C2H7N. D. C3H9N.
Giải:
\(n_{CO_{2}}=\frac{16,8}{22,4}=0,75\, mol\)
\(n_{N_{2}}=\frac{2,8}{22,4}=0,125\, mol\)
\(n_{H_{2}O}=\frac{20,25}{18}=1,125\, mol\)
\(C_{x}H_{y}N\rightarrow xCO_{2}+\frac{y}{2}H_{2}O+\frac{1}{2}N_{2}\)
amol \(\rightarrow\) a/2
\(n_{N_{2}}=\frac{a}{2}=0,125\, mol\Rightarrow \, n_{amin}=0,25\)
\(\frac{n_{CO_{2}}}{n_{amin}}=C=3\)
\(\frac{2.n_{H_{2}O}}{n_{amin}}=H=\frac{1,125.2}{0,25}=9\)
\(\Rightarrow C_{3}H_{9}N\)
\(\mathbf{\Rightarrow }\) Chọn câu D.
Bài tập 2: Đốt cháy hoàn toàn 0,1mol hỗn hợp gồm metylamin, đimetylamin, trimetylamin và etylamin bằng oxi vừa đủ thì thể tích N2 thu được (ở đktc) là
A. 4,48 lít B. 2,24 lít C. 1,12 lít D. 3,36 lít
Giải:
\(0,1 \, mol\left\{\begin{matrix} CH_{3}NH_{2}\\ (CH_{3})_{2}NH \\ (CH_{3})_{3}N \end{matrix}\right.\rightarrow N_{2}\)
\(C_{\bar{x}}H_{\bar{y}}N\,\, \, \, \rightarrow \, \frac{1}{2}N_{2}\)
0,1 mol \(\rightarrow\) 0,5 mol
\(V_{N_{2}}=0,05.22,4=1,12(l)\)
\(\mathbf{\Rightarrow }\) Chọn câu C.
Bài tập 3: Đốt cháy hoàn toàn hỗn hợp 2 amin no, đơn chức, mạch hở là đồng đẳng liên tiếp thu được 2,24 lít khí CO2 (đktc) và 3,6 H2O. Công thức của 2 amin là
A. CH3NH2 và C2H5NH2.
B. C2H5NH2 và C3H7NH2.
C. C3H7NH2 và C4H9NH2
D. C5H11NH2 và C6H13NH2.
Giải:
\(C_{\bar{n}}H_{2\bar{n}+3}N\rightarrow \bar{n}CO_{2}+(\frac{2\bar{n}+3}{2})H_{2}O\)
0,1 0,2
\(n_{CO_{2}}= 0,1 \, mol\)
\(n_{H_{2}O}= \frac{3,6}{18}=0,2 \, mol\)
\(\Rightarrow \frac{\bar{n}}{0,1}=\frac{2\bar{n}+3}{2.0,2}\, \Rightarrow \bar{n}=1,5\)
\(1<\bar{n}=1,5<2\left\{\begin{matrix} CH_{3}NH_{2}\\ C_{2}H_{5}NH_{2} \end{matrix}\right.\)
\(\mathbf{\Rightarrow }\) Chọn câu A.
Bài tập 4: Khi đốt cháy hoàn toàn một amin đơn chức X, thu được 8,4 lít khí CO2, 1,4 lít khí N2 (các thể tích khí đo ở đktc) và 10,125 gam H2O. Công thức phân tử của X là
A. C3H7N B. C2H7N C. C3H9N D. C4H9N
Giải:
\(C_{x}H_{y}N\rightarrow xCO_{2}+H_{2}O+\frac{1}{2}N_{2}\)
\(a\, \, \, \, \, \rightarrow\, \, \, \, \, \, \,\, \, \, \, \, \, \, \, \, \, \, \, \, \,\, \, \, \, \, \,\, \, \, \, \, \, \, \, \, \, \,\,\frac{a}{2}=0,0625\, mol\)
\(n_{CO_{2}}=\frac{8,4}{22,4}=0,375\, mol\)
\(n_{H_{2}O}=\frac{10,125}{18}=0,5625\, mol\)
\(a= 0,0625.2=0,125\, mol\)
\(\frac{n_{CO_{2}}}{n_{amin}}=3\left ( C \right )\)
\(\frac{2.n_{H_{2}O}}{n_{amin}}=\frac{0,5625.2}{0,125}=9(H)\)
\(\Rightarrow C_{3}H_{9}\)
\(\mathbf{\Rightarrow }\) Chọn câu C.
Bài tập 5: Hỗn hợp M gồm một anken và hai amin no, đơn chức, mạch hở X và Y là đồng đẳng kế tiếp nhau (MX < MY). Đốt cháy hoàn toàn một lượng M cần dùng vừa đủ 0,225 mol O2, thu được H2O, N2 và 0,12 mol CO2. Công thức phân tử của Y là
A. C3H9N. B. C2H7N. C. C4H11N. D. CH5N.
Giải:
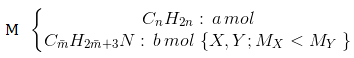
\(M+O_{2}\rightarrow H_{2}O+N_{2}+CO_{2}\)
( 0,225) (0,12)
\(C_{n}H_{2n}+\frac{3n}{2}O_{2}\rightarrow nCO_{2}+nH_{2}O\)
\(a\, \, \,\, \, \rightarrow \frac{3na}{2}\, \, \,\, \rightarrow na\)
\(C_{\bar{m}}H_{2\bar{m}+3}N+\left ( \frac{6\bar{m}+3}{4} \right )O_{2}\rightarrow \bar{m}CO_{2}+(\frac{2\bar{m}+3}{2})H_{2}O+\frac{1}{2}N_{2}\)
\(b\, \, \, \, \, \, \rightarrow \left ( \frac{6\bar{m}+3}{4} \right )b\, \rightarrow\,\, \, \, \bar{m}b\)
\(\left.\begin{matrix} \frac{3na}{2}+(\frac{6\bar{m}+3}{4})b=0,225\\ na+\bar{m}b=0,12 \end{matrix}\right\}b=0,06\)
\(\circledast \Rightarrow na+0,06\bar{m}=0,12\)
Nếu: \(\bar{m}>2 \Rightarrow na<0\) ( loại)
\(1<\bar{m}<2\left\{\begin{matrix} CH_{5}N\\ C_{2}H_{7}N :\, Y\end{matrix}\right.\)
\(\mathbf{\Rightarrow }\) Chọn câu B.
Bài tập 6: Đốt cháy hoàn toàn amin đơn chức X bằng không khí vừa đủ (gồm 20% thể tích là O2, còn lại là N2). Sản phẩm cháy cho qua bình nước vôi trong dư thấy 10,92 lít khí (đktc) thoát ra khỏi bình. Khối lượng bình tăng 4,875 gam và xuất hiện 7,5 kết tủa . Công thức phân tử của X là:
A. C2H7N B. C3H9N C. C6H7N D. C3H7N
Giải:
CXHyN: ( a mol)
\(C_{x}H_{y}N\overset{KK}{\rightarrow}CO_{2}+H_{2}O+N_{2}\)
Khí thoát ra là N2:
\(n_{N_{2}}=\frac{10,92}{22,4}=0,4875\)
\(n_{N_{2}}=n_{N}_{2}(_{KK})+n_{N}_{2}(_{amin})\)
.png)
\(4,875= 0,075.44+m_{H_{2}O}\)
\(\Rightarrow m_{H_{2}O}=1,575\, \left (g \right )\, \Rightarrow n_{H_{2}O}=0,0875\)
\(n_{N_{2}}\left ( _{KK} \right )=4.n_{O_{2}}\) (đ/c)
\(\Rightarrow n_{O_{2}}=0,075+\frac{0,0875}{2}=0,11875\)
\(n_{N_{2}}_{\left ( KK \right )}=4.0,11875=0,475\, mol\)
\(\circledast \Rightarrow \frac{a}{2}=0,4875-0,475\Rightarrow a=0,25\)
\(\Rightarrow C=\frac{0,075}{0,025}=3\)\(\Rightarrow C=\frac{0,075}{0,025}=3;\, H=\frac{0,0875.2}{0,025}=7\)
\(\Rightarrow C_{3}H_{7}N\)
\(\mathbf{\Rightarrow }\) Chọn câu D.














 Ra mắt HOC247 Kids nền tảng học tập Online #1
Ra mắt HOC247 Kids nền tảng học tập Online #1



